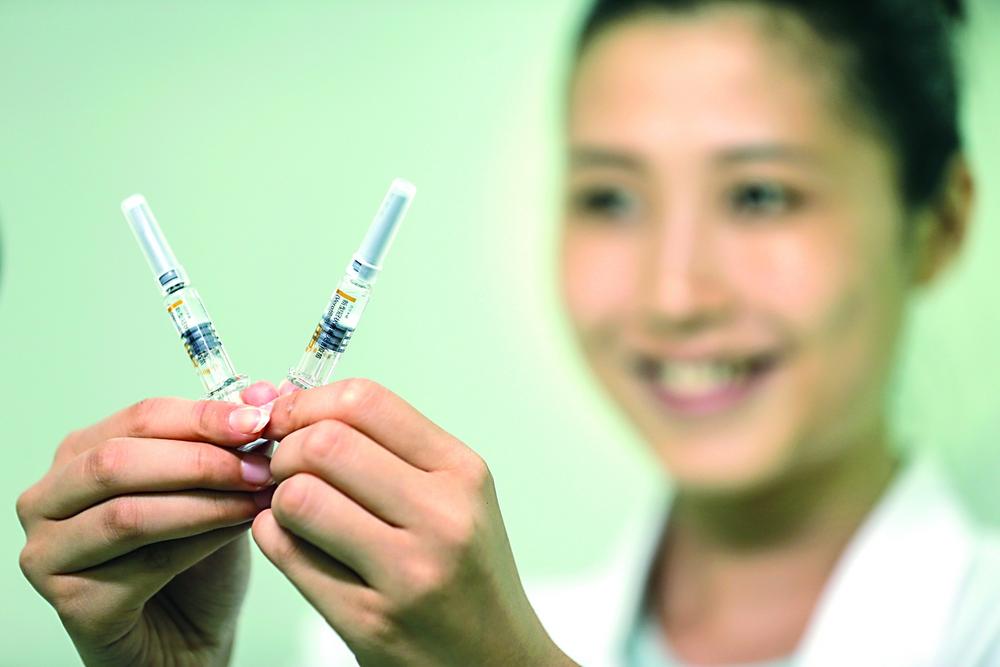
科興新冠疫苗獲附條件上市
據香港中通社、界面新聞報道:中國國家藥監局六日消息稱,國家藥品監督管理局於五日附條件批准北京科興中維生物技術有限公司的新型冠狀病毒滅活疫苗(Vero細胞),商品名稱“克爾來福”上市註冊申請。
本報綜合報道
滾動提交註冊資料
國家藥監局根據《疫苗管理法》、《藥品管理法》相關規定,按照藥品特別審批程序,進行應急審評審批,附條件批准上市註冊申請。國家藥監局要求該疫苗上市許可持有人繼續開展相關研究工作,完成附條件的要求,及時提交後續研究結果。
上述獲批上市的疫苗由科興控股子公司科興中維研製。科興中維自去年九月開始向國家藥品監督管理局藥品審評中心滾動提交註冊資料,藥監局按照研審聯動、隨提交隨審評的工作機制同步開展滾動審評。截至今年二月四日公司共計滾動提交四十餘次資料。
據科興中維網站資料顯示,“克爾來福”是用新型冠狀病毒(CZ02株)接種非洲綠猴腎細胞,經培養、收獲病毒液、滅活病毒、濃縮、純化和氫氧化鋁吸附製成,不含防腐劑。該疫苗適用於十八歲及以上人群的預防接種,用於預防新型冠狀病毒感染所致的疾病。該疫苗的基礎免疫程序為兩劑次,間隔十四至二十八天;每一次人用劑量為○點五毫升。
公佈三期臨床數據
二月五日,北京科興中維生物技術有限公司公佈其所研製的新型冠狀病毒滅活疫苗“克爾來福”的Ⅲ期臨床研究數據。結果顯示,通過在巴西、土耳其的Ⅲ期臨床研究,疫苗對預防新冠病毒所致疾病的保護效力均在百分之五十以上,最高可達百分之九十一點二五。
多國批准緊急使用
去年六月“克爾來福”在中國獲批緊急使用,並自七月開始陸續在國內針對特定人群開展緊急使用。
今年一月以來,印度尼西亞、土耳其、巴西、智利、哥倫比亞、烏拉圭和老撾等國陸續批准“克爾來福”在當地的緊急使用,目前多個國家針對醫務人員、老年人等高危人群已經陸續開展疫苗的接種工作。相關國家均認可科興中維現有臨床研究結果,認為該疫苗對於減少新冠病毒感染所致疾病導致的就醫、住院、重症及死亡有明顯作用,對疫情防控具有重要意義。
科興控股董事長尹衛東表示,“克爾來福”在國內獲批附條件上市標誌着持續一年的“克冠行動”取得了巨大的進展。據悉,科興中維將繼續積極推進“克爾來福”的三期臨床研究和附條件上市後的臨床研究,以及在相關國家和地區的註冊和應用。